II DOSSIER MEDICAL : AUJOURD'HUI VOUS SAUREZ TOUT SUR LA PANDEMIE DU CORONAVIRUS - COVID-19 ( suite )
| Type | Virus |
|---|---|
| Domaine | Riboviria |
| Ordre | Nidovirales |
| Sous-ordre | Cornidovirineae |
| Famille | Coronaviridae |
Genres de rang inférieur
- AlphacoronavirusAlphacoronavirus
- Betacoronavirus
- Gammacoronavirus (en)
- Deltacoronavirus (en)
Les coronavirus (abrégé en CoV ; du latin signifiant « virus à couronne »)[réf. nécessaire], ou Orthocoronavirinae, constituent une sous-famille de virus de la famille des Coronaviridae. Le virus à couronne[réf. nécessaire] doit son nom à l'apparence des virions sous un microscope électronique, avec une frange de grandes projections bulbeuses qui ressemblent à la couronne solaire.
Les coronavirus sont munis d'une enveloppe virale ayant un génome à ARN de sens positif et une capside (coque) kilobases, incroyablement grosse pour un virus à ARN. Ils se classent parmi les Nidovirales, puisque tous les virus de cet ordre produisent un jeu imbriqué d'ARNm sous-génomique lors de l'infection. Des protéines en forme de pic, enveloppe, membrane et capside contribuent à la structure d'ensemble de tous les coronavirus. Ces virus à ARN sont monocaténaires (simple brin) et de sens positif (groupe IV de la classification Baltimore). Ils peuvent muter et se recombiner[2].
Les chauves-souris et les oiseaux, en tant que vertébrés volants à sang chaud, sont des hôtes idéaux pour les coronavirus assurant l'évolution et la dissémination du coronavirus[3]. Les coronavirus sont normalement spécifiques à un taxon animal comme hôte, mammifères ou oiseaux selon leur espèce ; mais ces virus peuvent parfois changer d'hôte à la suite d'une mutation. Leur transmission interhumaine se produit principalement par contacts étroits via des gouttelettes respiratoires générées par les éternuements et la toux.
Les coronavirus ont été responsables chez l'homme des graves épidémies de syndrome respiratoire aigu sévère (SRAS) en 2002/2003 et du syndrome respiratoire du Moyen-Orient (MERS) à partir de 2012, ainsi que la pandémie de Covid-19 de 2020, causée par le coronavirus SARS-CoV-2, contre lequel on ne dispose pas encore de vaccin ni de médicament à l'efficacité prouvée.
Sommaire
Caractérisation
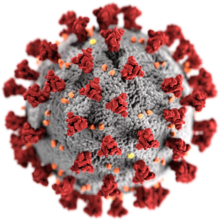
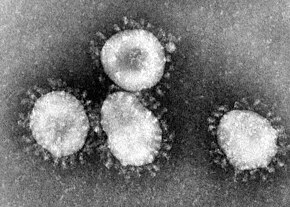
Les coronavirus ont été découverts dans les années 1960[4]. Les premiers découverts furent ceux de la bronchite infectieuse du poulet, puis deux virus des cavités nasales de patients humains atteints de rhume, ensuite nommés coronavirus humain 229E et coronavirus humain OC43.
Le terme coronavirus (du latin corona et virus, littéralement « virus à couronne ») provient de l'apparence des virions au microscope électronique, caractérisée par une frange de grandes protubérances entourant l'enveloppe avec l'apparence d'une couronne, par analogie avec la couronne solaire.
Les hôtes idéaux des coronavirus, en tant que vertébrés volants à sang chaud, sont les chauves-souris (pour les Alphacoronavirus et les Betacoronavirus) et les oiseaux (pour les Gammacoronavirus (en) et les Deltacoronavirus (en)). Ces espèces-réservoir assurent l'évolution et la dissémination des coronavirus[3]. Chez d'autres espèces, les symptômes varient (maladies des voies respiratoires supérieures chez la poule, diarrhée chez la vache ou le porc).
L'être humain abrite naturellement quatre types de coronavirus bénins, qui provoquent des infections des voies respiratoires, comme le rhume, et plus rarement affectent les systèmes gastro-intestinaux, cardiaques et nerveux[5].
Les groupes de coronavirus ont normalement un hôte animal spécifique (mammifères, oiseaux ou reptiles[6]) mais ils peuvent parfois changer d'hôte à la suite d'une mutation. De telles mutations ont provoqué chez l'homme les graves épidémies de SRAS en 2002/2003 et du syndrome respiratoire du Moyen-Orient en 2012, ainsi que la pandémie de 2019-2020 de COVID-19 (causée par le coronavirus SARS-CoV-2).
Biologie
Ce virus enveloppé est constitué d'une enveloppe virale entourant une capside hélicoïdale qui contient le brin d'ARN. La taille du génome de ces virus varie d'environ 26 à 32 kilobases, valeurs parmi les plus élevées chez les virus à ARN.
Les coronavirus ont en commun des protéines désignées par une lettre indiquant leur localisation : S (protubérances), E (enveloppe), M (membrane) et N (nucléocapside). Certains, notamment ceux du sous-groupe A du genre Betacoronavirus, ont une protéine HE (hémagglutinine estérase (en)) caractéristique. Le coronavirus du SRAS présente en outre sur la protéine S un site de liaison spécifique à l'enzyme de conversion de l'angiotensine 2[7] qui lui sert de point d'entrée dans la cellule hôte.
La taille physique du virion est classiquement donnée comme étant de 120 à 160 nm[8] ou comme étant de l'ordre de 125 nm[9]. Toutefois le SARS-CoV-2, responsable du Covid-19 a été annoncé plus récemment comme mesurant approximativement de 60 à 140 nm, et comme étant de forme elliptique avec de nombreuses variations[10].
Elle se fait en six étapes successives (voir illustration) :
- Grâce à leur protéine S, les coronavirus se lient aux molécules cellulaires de surface telles que les métalloprotéinases. Les virus dotés en plus de la protéine HE (hémagglutinine-estérase) dans leur enveloppe peuvent aussi se lier à l'acide N-acétylneuraminique qui sert de corécepteur (lui-même initiateur de l'entrée d'un pathogène dans une cellule hôte). On ne sait pas clairement si les virus entrent dans la cellule hôte par fusion des membranes virales et cellulaires, ou par une internalisation à récepteur. Quel qu’en soit le mécanisme, le brin d'ARN est inséré dans la cellule, et la capside (la coque) est abandonnée.
- Les coronavirus sont munis d'un seul génome ARN à brin positif, à présent sur place dans le cytoplasme. Le génome de l'ARN du coronavirus a une coiffe méthylée 5 'et une queue polyadénylée 3', ce qui permet à l'ARN de se fixer aux ribosomes pour la traduction. Les ribosomes de la cellule décodent l'ARN viral, produisant les protéines qui y sont codées.
- D'abord l'ARN positif du virus est transcrit en protéine pour former une ARN polymérase propre (une ARN polymérase ARN-dépendante). La réplicase est la première protéine fabriquée ; une fois le gène codant la réplicase traduit par le ribosome de la cellule hôte, la traduction est arrêtée par un codon stop. Cette réplicase virale ne reconnaît et produit que l'ARN viral, et permet au génome viral d'être transcrit en nouvelles copies d'ARN, à l'aide de la machinerie de la cellule hôte. Se servant du brin positif comme modèle, cet enzyme assemble le brin négatif.
- Par la suite, ce brin négatif sert lui-même de modèle pour transcrire de petits ARN sous-génomiques, qui sont utilisés pour fabriquer toutes les autres protéines. C'est ce qu'on appelle une transcription imbriquée. Ce processus est une forme d'économie génétique, permettant au virus de coder le plus grand nombre de gènes dans un petit nombre de nucléotides.
Le génome du brin négatif est traduit par le ribosome de la cellule hôte, et une longue polyprotéine est formée, où toutes les protéines virales sont attachées. Les coronavirus ont une protéine non structurale - une protéase - qui est capable de cliver la polyprotéine.
Par ailleurs, ce brin négatif joue un rôle dans la réplication de nouveaux génomes ARN à brin positif.
Le cytoplasme de la cellule hôte se remplit de protéines et d'ARN viraux. - (a) La protéine N aide à lier l'ARN génomique pour réaliser l’encapsidation du génome virale dans une enveloppe protectrice nommée capside[11] ; la protéine M s'intègre à la membrane du réticulum endoplasmique, côté capside ; et des protéines HE et S traversent la membrane du réticulum endoplasmique, via la protéine de translocation, et se positionnent du côté opposé.
(b) Avec la liaison entre la capside et les protéines M, la membrane du réticulum s'invagine, et bourgeonne. La capside (la coque) assemblée dotée d'ARN hélicoïdal se retrouve alors à l'intérieur du réticulum endoplasmique, ayant capturé à son profit la membrane de ce dernier, qui porte à présent à son extérieur les protéines HE et S. - Cette progéniture virale est ensuite (a) encapsulée et transportée par des vésicules golgiennes vers la membrane cellulaire, (b) pour être enfin externalisée (par exocytose) hors de la cellule.
Sept types de coronavirus infectent couramment l'homme[12], dont quatre sans gravité et trois causant des infections graves.
Les infections bénignes sont des rhumes avec fièvre et des maux de gorge dus à des végétations adénoïdes gonflées, principalement en hiver et au début du printemps[13].
Les coronavirus seraient la cause de 15 à 30 % des rhumes courants[14]. Chez l'Homme, ce sont : 229E, NL63, OC43, et HKU1 : quatre types de coronavirus inconnus chez la chauve-souris.
Des coronavirus qui ne se trouvent pas naturellement chez l'homme mais chez des mammifères ont été à l'origine d'infections graves des poumons (pneumopathie virale) :
- le SARS-CoV, pour l'épidémie de syndrome respiratoire aigu sévère lié au coronavirus (SRAS) en 2003 qui a déclenché une alerte mondiale de l'OMS. Elle a débuté en Chine en 2002 après la consommation dans un restaurant d'un animal sauvage, la civette palmiste masquée. La maladie a fait 774 morts (10 % environ des personnes atteintes). Elle est considérée comme éradiquée depuis 2004.
- le MERS-CoV, pour l'épidémie de syndrome respiratoire du Moyen-Orient qui a débuté en Arabie saoudite en 2012. Son taux de mortalité a été de 35 %, faisant [Quand ?]449 victimes seulement du fait du faible nombre d'individus atteints. [réf. nécessaire]Elle aurait été déclenchée par la consommation de lait de chameau et par la proximité avec les chameaux. Cette maladie existe toujours car pour pouvoir l'éradiquer, il faudrait que les populations qui utilisent traditionnellement des chameaux puissent s'en passer.
- Le SARS-CoV-2, pour la pandémie de Covid-19 (maladie à coronavirus 2019) qui est apparue en Chine en 2019 et s'est étendue dans le monde entier en 2020. La consommation de viande de pangolin[15] et de chauve-souris (vendues pour l'alimentation en Chine) pourrait en être à l'origine.
Selon le virus en cause, les formes graves de la maladie ont leurs particularités. Par exemple, la diarrhée était très fréquente dans le SRAS mais rare dans la maladie à coronavirus 2019.
Trois principales sources sont utilisées : l'Institut Pasteur, l'OMS et les CDC américains[16].
| Syndrome respiratoire du Moyen-Orient (MERS)[17],[18] | Syndrome respiratoire aigu sévère (SRAS)[19],[20],[21] | Maladie à coronavirus 2019 (COVID-19) | |
|---|---|---|---|
| Agent pathogène | MERS-CoV | SARS-CoV | SARS-CoV-2 |
| Année d'apparition | 2012 | 2003 | 2019 |
| Nombre de cas | 1 219 | 8 098 dont 5 327 en Chine. | En cours, voir ici |
| Pourcentage de cas par transmission nosocomiale | 70 %[22] | 58 %[22] | |
| Nombre de décès | 449 | 774 (dont 349 en Chine) | En cours, voir ici |
| Réservoir | Dromadaire | Chauve-souris | Chauve-souris (probablement) |
| Transmission à l'homme par l'animal | Contact direct avec un animal infecté, consommation de lait cru de dromadaire. | Consommation de viande de civette palmiste masquée, animal sauvage vendu sur les marchés et consommé au sud de la Chine. | Pangolin[15] serait l'hôte intermédiaire. |
| Transmission interhumaine | Oui | Oui | Oui |
| Transmission par objet | – | Oui | Risque très faible. |
| Transmission materno-fœtale | – | Aucun cas retrouvé chez les femmes enceintes infectées par ce virus[23]. | Aucune preuve[24]. |
| Incubation | Entre 5 et 15 jours. | Entre 2 et 7 jours. | Probablement moins de 14 jours, mais pouvant aller jusqu'au double[25]. |
| Porteur sain | – | Probablement pas. | Oui, |
| Fièvre | Très fréquente mais peut apparaître plusieurs jours après la toux ou les difficultés à respirer. | ||
| Contagiosité | Taux de reproduction inférieur à 1[26]. | Taux de reproduction supérieur à 2[26]. | Taux de reproduction de base entre 1,4 et 5,4[27],[28],[29], à confirmer. |
| Durée de la contagiosité | – | – | Semble limitée à la période des signes cliniques. Possibilité disputée de contagion en phase asymptomatique[30]. |
| Début de la période de contagiosité | – | 3 à 4 jours après le début des signes cliniques. | Dès l'apparition des signes cliniques. Possibilité disputée de contagion en phase asymptomatique[30]. |
| Diarrhée | Signes cliniques fréquents jusque 50 % des cas[23]. | Oui mais proportion faible 10 %. | |
| Transmission par les selles | Très probable mais a joué un rôle mineur[23]. | Cette possibilité est envisagée[31]. | |
| Létalité | 34,4 %[22] | 9,5 %[22] , au-delà de 50 % chez les plus de 65 ans. | 3,4 %[32] |
| Traitement | Symptomatique | Symptomatique | Symptomatique |
| Vaccin | Aucun | Aucun | Aucun |
| Statut | Résurgence possible. | Considéré comme éradiqué. | Épidémie en cours. |
Au vu des séquences génomiques disponibles, deux grands taxons animaux seraient le réservoir principal des CoVs :
- chiroptères : hôtes naturels du HCoV-NL63 et du HCoV-229E[33] ;
- rongeurs : hôtes naturels du HCoV-OC43 et HKU1[33].
Au vu des connaissances disponibles, les coronavirus semblaient avoir besoin d'hôtes intermédiaires (toujours des mammifères) pour s'« humaniser », c'est-à-dire muter pour pouvoir infecter l'Homme.
Des hôtes intermédiaires connus ont été :
- des bovins pour HCoV-OC43 [33] ;
- l'alpaga pour HCoV-229E [33] ;
- la civette masquée pour le SRAS-CoV[33] ;
- le dromadaire pour le MERS-CoV [33].
Pour la pandémie de 2019-2020 voir les articles suivants :
La transmission interhumaine des coronavirus se fait principalement par les gouttelettes ou des aérosols respiratoires expectorées par une personne infectée (via la toux, les éternuements, des postillons, ou parfois par le simple fait de parler fort ou en criant) quand les particules virales sont inhalées par une personne se trouve à proximité. La transmission et la contagiosité varient aussi selon le coronavirus, et peut-être selon sa souche au sein d'une épidémie.
La prophylaxie passe par une prévention primaire visant à limiter la transmission du virus : éviter les contacts (surfaces potentiellement contaminées, poignées de main, embrassades), se laver les mains fréquemment, éviter de se toucher les yeux, le nez ou la bouche, par où le virus peut s'introduire dans l'organisme. En cas de symptômes de type toux ou rhume, se maintenir à au moins 1 mètre de toute personne et éviter d'émettre des particules contaminées[34].
D'autres recommandations comprennent[35] :
- ne pas entrer en contact avec des animaux manifestement malades, ne pas consommer de viandes provenant d'animaux malades ;
- ne pas consommer de produits animaux (viande...) mal cuits, ni de légumes crus s'ils n'ont pas été lavés avec de l'eau non contaminée.
Comme tous les virus, le coronavirus est insensible aux antibiotiques et aux préparations bactériophagiques, qui ne peuvent être utiles que contre les surinfections bactériennes.
Dans le cas du SRAS, des médicaments ont été utilisés pour tenter d'enrayer l'épidémie : la ribavirine, un analogue de nucléotides, des anti-inflammatoires stéroïdiens et, après identification formelle de l'agent pathogène et des criblages de sensibilité, l'interféron-alpha et des inhibiteurs de protéases. Leur efficacité est encore sujette à caution. Aucun n'a fait l'objet d'une étude clinique adéquate : beaucoup d'études disponibles ne permettent pas de conclusions scientifiques claires car elles ont été réalisées sur de petits nombres de sujets ou alors sans protocole ou dose fixe. Certaines indiquent même que ces traitements pourraient avoir nui à l'éradication du virus[36].
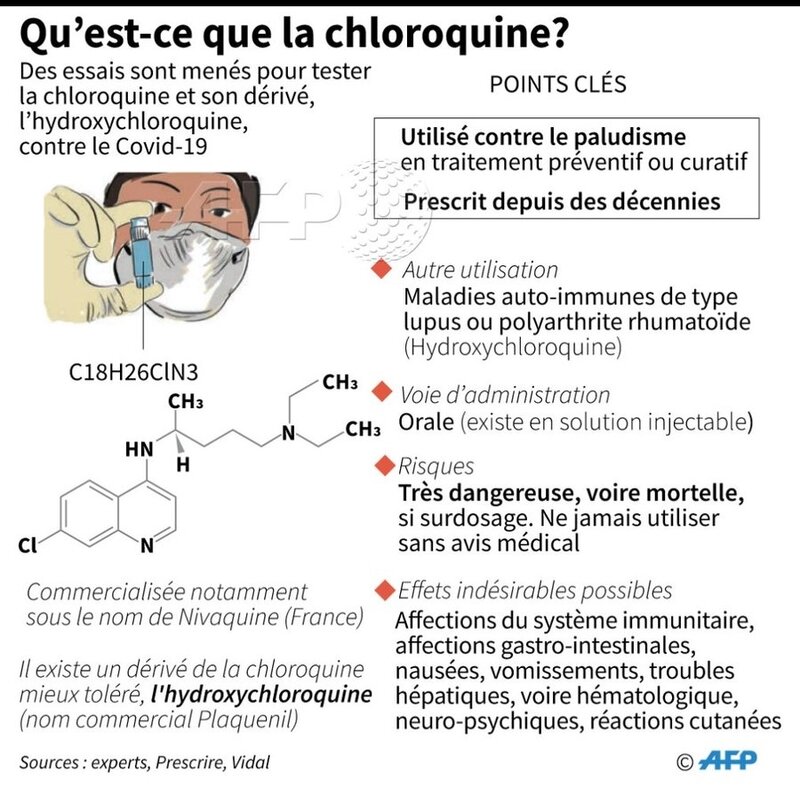
Dans le cas de la Covid-19, les pistes de traitement[37] comprennent l'administration de chloroquine ou d'hydroxychloroquine, efficaces in vitro (tests en laboratoire)[38] mais toxiques à haute dose in vivo (en conditions réelles sur l'homme) [39]. Des études en Chine et un premier essai thérapeutique en France, mené à l'institut hospitalo-universitaire de Marseille se sont montrés prometteurs, mais font l'objet d'essais plus étendus afin de confirmer leur efficacité et leur incocuité[40].
L'éradication rapide de l'épidémie de SRAS précédente n'a pas laissé place à beaucoup d'essais cliniques. Des vaccins à base de virus inactivé, et d'autres fondés sur les protéines S et N, sont à l'étude depuis plusieurs années[41].
Taxinomie
Les coronavirus sont nommés par un groupe d'étude [42] travaillant au sein de l'ICTV (International committee on Taxonomy of viruses)[43].
Les coronavirus (CoV) sont des virus à ARN monocaténaire de sens positif (groupe IV de la classification Baltimore) correspondant à la sous-famille Orthocoronavirinae de la taxonomie de l'ICTV[1], dans la famille des Coronaviridae, de l'ordre des Nidovirales et du royaume des Riboviria[44],[45].
Quatre genres contiennent des virus pathogènes pour les mammifères[2] :
- Alphacoronavirus, qui inclut le virus de la diarrhée épidémique porcine (PEDv), le virus de la gastro-entérite transmissible (TGEV), le coronavirus du syndrome de la diarrhée aiguë porcine (SADS-CoV), le coronavirus entérique canin, le coronavirus entérique félin, le virus de la péritonite infectieuse féline (FIPV) ;
- Bétacoronavirus, dont le virus respiratoire-respiratoire du SRAS (SARS-CoV), le SARS-CoV-2, le coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV), virus de l'hépatite murine (MHV), coronavirus bovins, virus de la sialodacryoadénite du rat, virus de la sialodacryoadénite porcine, hémagglutinose porcine, virus de l'hémagglutinose porcine coronavirus équin.
Dans ce genre Betacoronavirus, le SARS-CoV et le SARS-CoV-2 appartiennent tous les deux au sous-genre Sarbecovirus au sein duquel 3 clades distincts ont été identifiés :
o Clade1: batSARSr-CoVstrainsdeBulgariaandKenya[46]
o Clade2: SARS-CoV-2etbatSARSr-CoVstrainsfreasteastChina[46]
o Clade3: SARS-CoVandbatSARSr-CoVstrainsfromsouthwesternChina[46]
- Gammacoronavirus : surtout trouvé chez des oiseaux migrateurs, causant notamment des bronchites ; un Gammacoronavirus a été isolé d'un béluga en captivité
- Deltacoronavirus: connus depuis peu, qui semblent surtout infecter les oiseaux, mais aussi trouvé chez les porcs.
Remarques : On nomme parfois un coronavirus selon l'espèce animale où on l'a trouvé (par exemple : coronavirus respiratoire canin, ou CRCoV pour Canine respiratory coronavirus, virus appartenant au genre betacoronavirus et à son sous-groupe 2a)[47],[48].
Le dernier coronavirus trouvé, pandémique, en 2020, est le SARS-CoV-2
La sous-famille Orthocoronavirinae de la famille Coronaviridae est organisée en 4 genres, 22 sous-genres et une quarantaine d'espèces[49]:
- Sous-famille Orthocoronavirinae
- Genre Alphacoronavirus
- Sous-genre Colacovirus
- Bat coronavirus CDPHE15
- Sous-genre Decacovirus
- Bat coronavirus HKU10
- Rhinolophus ferrumequinum alphacoronavirus HuB-2013
- Sous-genre Duvinacovirus
- Human coronavirus 229E (en) (HCoV-229E)
- Sous-genre Luchacovirus
- Lucheng Rn rat coronavirus
- Sous-genre Minacovirus
- Ferret coronavirus
- Mink coronavirus 1
- Sous-genre Minunacovirus
- Miniopterus bat coronavirus 1
- Miniopterus bat coronavirus HKU8
- Sous-genre Myotacovirus
- Myotis ricketti alphacoronavirus Sax-2011
- Nyctacovirus
- Nyctalus velutinus alphacoronavirus SC-2013
- Sous-genre Pedacovirus
- Porcine epidemic diarrhea virus
- Scotophilus bat coronavirus 512
- Sous-genre Rhinacovirus
- Rhinolophus bat coronavirus HKU2
- Sous-genre Setracovirus
- Human coronavirus NL63 (en) (HCoV-NL63)
- NL63-related bat coronavirus strain BtKYNL63-9b
- Sous-genre Tegacovirus
- Alphacoronavirus 1
- Sous-genre Colacovirus
- Genre Betacoronavirus
- Sous-genre Embecovirus
- Betacoronavirus 1 (incl. Human coronavirus OC43 (en), HCoV-OC43)
- China Rattus coronavirus HKU24
- Human coronavirus HKU1 (en) (HCoV-HKU1)
- Murine coronavirus
- Sous-genre Hibecovirus
- Bat Hp-betacoronavirus Zhejiang2013
- Sous-genre Merbecovirus
- Hedgehog coronavirus 1
- Middle East respiratory syndrome-related coronavirus (MERS-CoV)
- Pipistrellus bat coronavirus HKU5
- Tylonycteris bat coronavirus HKU4
- Sous-genre Nobecovirus
- Rousettus bat coronavirus GCCDC1
- Rousettus bat coronavirus HKU9
- Sous-genre Sarbecovirus
- Sous-genre Embecovirus
- Genre Gammacoronavirus
- Sous-genre Cegacovirus
- Beluga whale coronavirus SW1
- Sous-genre Igacovirus
- Sous-genre Cegacovirus
- Genre Deltacoronavirus
- Sous-genre Andecovirus
- Wigeon coronavirus HKU20
- Sous-genre Buldecovirus
- Bulbul coronavirus HKU11
- Coronavirus HKU15
- Munia coronavirus HKU13
- White-eye coronavirus HKU16
- Sous-genre Herdecovirus
- Night heron coronavirus HKU19
- Sous-genre Moordecovirus
- Common moorhen coronavirus HKU21
- Sous-genre Andecovirus
- Genre Alphacoronavirus
Notes et références
- (en) « Virus Taxonomy: 2018b Release » [archive], ICTV, juillet 2018 (consulté le 24 janvier 2020).
- SARS-CoV, B. S. (2020). Mutation and Recombination [archive].
- (en) Patrick C. Y. Woo, Susanna K. P. Lau, Carol S. F. Lam, Candy C. Y. Lau, Alan K. L. Tsang, John H. N. Lau, Ru Bai, Jade L. L. Teng, Chris C. C. Tsang, Ming Wang, Bo-Jian Zheng, Kwok-Hung Chan et Kwok-Yung Yuen, « Discovery of Seven Novel Mammalian and Avian Coronaviruses in the Genus Deltacoronavirus Supports Bat Coronaviruses as the Gene Source of Alphacoronavirus and Betacoronavirus and Avian Coronaviruses as the Gene Source of Gammacoronavirus and Deltacoronavirus », Journal of Virology, vol. 86, no 7, avril 2012, p. 3995-4008 (PMID 22278237, DOI 10.1128/JVI.06540-11, Bibcode 3302495, lire en ligne [archive], consulté le 6 mars 2020)
- (en-US) « Coronavirus: Common Symptoms, Preventive Measures, & How to Diagnose It » [archive], sur Caringly Yours, 28 janvier 2020 (consulté le 28 janvier 2020)
- Zhu N, Zhang D, Wang W et al., « A Novel Coronavirus from Patients with Pneumonia in China, 2019. », N Engl J Med 2020, {{Article}} : paramètre «
date» manquant. - Jacobson E.R (2007) Infectious Diseases and Pathology of Reptiles; CRC Press, Taylor & Francis Group: Boca Raton, FL, États-Unis ; p. 33487–2742 (lien Google Livre [archive])
- (en) Fang Li, Wenhui Li, Michael Farzan et Stephen C. Harrison, « Structure of SARS Coronavirus Spike Receptor-Binding Domain Complexed with Receptor », Science, vol. 309, no 5742, 16 septembre 2005, p. 1864-1868 (PMID 16166518, DOI 10.1126/science.1116480, JSTOR 3843779, Bibcode 2005Sci...309.1864L, lire en ligne [archive], consulté le 25 janvier 2020)
- (en) Thomas C. Holland, Neurovirology in Handbook of Clinical Neurology, 2014 lire en ligne [archive]
- (en) Fehr, Anthony R, Stanley Perlman. “Coronaviruses: an overview of their replication and pathogenesis.” Methods in molecular biology (Clifton, N.J.) vol. 1282 (2015): 1-23. doi:10.1007/978-1-4939-2438-7_1 lire en ligne [archive]
- Cascella M, Rajnik M, Cuomo A, et al. Features, Evaluation and Treatment Coronavirus (COVID-19), in: StatPearls [Internet], StatPearls Publishing, Treasure Island (Floride), janvier 2020, mis à jour le 8 mars 2020 lire en ligne [archive]
- (en) Ping-Kun Hsieh, Shin C. Chang, Chu-Chun Huang et Ting-Ting Lee, « Assembly of severe acute respiratory syndrome coronavirus RNA packaging signal into virus-like particles is nucleocapsid dependent », Journal of Virology, vol. 79, no 22, novembre 2005, p. 13848–13855 (ISSN 0022-538X, PMID 16254320, PMCID 1280188, DOI 10.1128/JVI.79.22.13848-13855.2005, lire en ligne [archive], consulté le 13 mars 2020)
- (en) CDC, « Human Coronavirus Types » [archive], sur Center for Disease Control Prevention (consulté le 22 janvier 2020)
- (en) « Prevalence and genetic diversity analysis of human coronaviruses among cross-border children », Virology Journal, vol. 14, no 1, novembre 2017, p. 230 (PMID 29166910, PMCID 5700739, DOI 10.1186/s12985-017-0896-0)
- « Coronaviruses: an overview of their replication and pathogenesis », Methods in Molecular Biology, vol. 1282, 2015, p. 1–23 (ISBN 978-1-4939-2437-0, PMID 25720466, PMCID 4369385, DOI 10.1007/978-1-4939-2438-7_1)
- L'hypothèse du pangolin javanais comme hôte intermédiaire du coronavirus [archive]
- Coronavirus Disease (COVID-19 [archive] cdc.gov, consulté le 02 mars 2020
- « MERS-CoV » [archive], Institut Pasteur, 6 octobre 2015 (consulté le 29 janvier 2020).
- (en-US) CDC, « Middle East Respiratory Syndrome (MERS) » [archive], sur Centers for Disease Control and Prevention, 2 août 2019 (consulté le 29 janvier 2020).
- « SRAS » [archive], Institut Pasteur, 6 octobre 2015 (consulté le 29 janvier 2020).
- O.M.S, « Syndrome aiguë respiratoire » [archive], sur O.M.S (consulté le 29 janvier 2020).
- (en-US) « SARS | Home | Severe Acute Respiratory Syndrome | SARS-CoV Disease | CDC » [archive], sur www.cdc.gov, 22 octobre 2019 (consulté le 29 janvier 2020).
- Vincent J. Munster, Marion Koopmans, Neeltje van Doremalen et Debby van Riel, « A Novel Coronavirus Emerging in China — Key Questions for Impact Assessment », The New England Journal of Medicine, vol. 382, no 8, 20 février 2020, p. 692–694 (ISSN 0028-4793, DOI 10.1056/NEJMp2000929, lire en ligne [archive], consulté le 3 mars 2020)
- World Health Organization, "Consensus document on the epidemiology of severe acute respiratory syndrome (SARS)", 2003, page 15.
- (en) Huijun Chen, Juanjuan Guo, Chen Wang et Fan Luo, « Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in nine pregnant women: a retrospective review of medical records », The Lancet, vol. 395, no 10226, 7 mars 2020, p. 809–815 (ISSN 0140-6736 et 1474-547X, PMID 32151335, DOI 10.1016/S0140-6736(20)30360-3, lire en ligne [archive], consulté le 27 mars 2020)
- « EN DIRECT - Coronavirus : la période d'incubation plus longue que prévu ? » [archive], sur LCI (consulté le 22 février 2020)
- (en) David L. Swerdlow et Lyn Finelli, « Preparation for Possible Sustained Transmission of 2019 Novel Coronavirus: Lessons From Previous Epidemics », JAMA, 11 février 2020 (ISSN 0098-7484, DOI 10.1001/jama.2020.1960, lire en ligne [archive], consulté le 12 février 2020)
- (en) Saey, Tina Hesman, « How the new coronavirus stacks up against SARS and MERS », ScienceNews, 24 janvier 2020 (lire en ligne [archive]).
- (en-GB) « Virus deaths rise as more cities restrict travel », BBC News, 24 janvier 2020 (lire en ligne [archive], consulté le 24 janvier 2020).
- (en) Shi Zhao, Jinjun Ran, Salihu S. Musa et Guangpu Yang, « Preliminary estimation of the basic reproduction number of novel coronavirus (2019-nCoV) in China, from 2019 to 2020: A data-driven analysis in the early phase of the outbreak », bioRxiv, 24 janvier 2020, p. 2020.01.23.916395 (DOI 10.1101/2020.01.23.916395, lire en ligne [archive], consulté le 29 janvier 2020).
- https://www.lemonde.fr/les-decodeurs/article/2020/02/06/coronavirus-une-affiche-du-ministere-ecarte-trop-vite-le-risque-de-contagion-lors-de-l-incubation_6028658_4355770.html [archive]
- « Coronavirus : la maladie pourrait aussi se transmettre par voie fécale » [archive], sur www.pourquoidocteur.fr (consulté le 17 mars 2020)
- « Coronavirus : L’OMS indique que le taux de mortalité est de 3,4 % », Intellivoire, 5 mars 2020 (lire en ligne [archive], consulté le 5 mars 2020).
- (en) Jie Cui, Fang Li et Zheng-Li Shi, « Origin and evolution of pathogenic coronaviruses », Nature Reviews Microbiology, vol. 17, no 3, mars 2019, p. 181–192 (ISSN 1740-1534, DOI 10.1038/s41579-018-0118-9, lire en ligne [archive], consulté le 17 mars 2020)
- Coronavirus disease (COVID-19) advice for the public [archive], OMS, 2020.
- « Coronavirus – informations et conseils » [archive], sur Centre de vaccinations internationales Air France (consulté le 13 mars 2020)
- Stockman LJ, Bellamy R, Garner P. SARS: systematic review of treatment effects [archive]. PLoS Med. 2006;3:e343. doi:10.1371/journal.pmed.0030343
- (en) Franck Touret et Xavier de Lamballerie, « Of chloroquine and COVID-19 », Antiviral Research, vol. 177, 1er mai 2020, p. 104762 (ISSN 0166-3542, DOI 10.1016/j.antiviral.2020.104762, lire en ligne [archive], consulté le 17 mars 2020)
- Manli Wang, Ruiyuan Cao, Leike Zhang et Xinglou Yang, « Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro », Cell Research, vol. 30, no 3, mars 2020, p. 269–271 (ISSN 1748-7838, PMID 32020029, PMCID 7054408, DOI 10.1038/s41422-020-0282-0, lire en ligne [archive], consulté le 17 mars 2020)
- « La chloroquine, une piste pour lutter contre le SARS-CoV-2 », Le Monde.fr, 17 mars 2020 (lire en ligne [archive], consulté le 17 mars 2020)
- Journal Le Soir, Belgique, Bruxelles, 17 mars 2020
- Zhu, M. 2004. SARS immunity and vaccination [archive]. Cell. Mol. Immunol. 1:193-198
- coronavirus Study Group ou CSG
- Gorbalenya A.E & a. (2020) Severe acute respiratory syndrome-related coronavirus: The species and its viruses – a statement of the Coronavirus Study Group. bioRxiv, https://www.biorxiv [archive]. org/content/10.1101/2020.02.07.937862v1.full.pdf.
- Ninth Report of the International Committee on Taxonomy of Viruses, Oxford, Elsevier, 2011, 806–828 p. (ISBN 978-0-12-384684-6), « Family Coronaviridae »
- International Committee on Taxonomy of Viruses, « ICTV Master Species List 2009 – v10 » [archive] [xls], 24 août 2010
- Lu R, Zhao X, Li J, Niu P, Yang B, Wu H, [...] Tan W, 2020. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. The Lancet doi: https://doi.org/10.1016/S0140-6736(20)30251-8 [archive].
- (en) Kerstin Erles, Kai-Biu Shiu et Joe Brownlie, « Isolation and sequence analysis of canine respiratory coronavirus », Virus Research, vol. 124, no 1, 1er mars 2007, p. 78–87 (ISSN 0168-1702, DOI 10.1016/j.virusres.2006.10.004, lire en ligne [archive], consulté le 17 mars 2020)
- (en) Kerstin Erles, Crista Toomey, Harriet W Brooks et Joe Brownlie, « Detection of a group 2 coronavirus in dogs with canine infectious respiratory disease », Virology, vol. 310, no 2, 5 juin 2003, p. 216–223 (ISSN 0042-6822, DOI 10.1016/S0042-6822(03)00160-0, lire en ligne [archive], consulté le 17 mars 2020)
- (en) « Virus taxonomy: 2018b release » [archive], sur ICTV online, juillet 2018 (consulté le 24 janvier 2020)
Voir aussi
- (en) Christine V.F. Carrington, Jerome E. Foster, Hua Chen Zhu, Jin Xia Zhang, Gavin J.D. Smith, Nadin Thompson, Albert J. Auguste, Vernie Ramkissoon, Abiodun A. Adesiyun et Yi Guan, « Detection and Phylogenetic Analysis of Group 1 Coronaviruses in South American Bats », Emerging Infectious Diseases journal, Centers for Disease Control and Prevention, vol. 14, no 12, décembre 2008, p. 1890-1893 (DOI 10.3201/eid1412.080642, lire en ligne [archive])
- Saif, L. J., Wang, Q., Vlasova, A. N., Jung, K., & Xiao, S. (2019). Coronaviruses [archive]. Diseases of swine, 488-523.
- Frédérique Schneider, « Coronavirus, les chiffres de l’épidémie » [archive], sur La Croix, 17 février 2020 (consulté le 18 février 2020)
- Xavier Olessa-Daragon, Fiene Marie Kuijper, « 10 points sur le Coronavirus COVID-19 » [archive], sur Le Grand Continent, 26 janvier 2020 (consulté le 28 février 2020).
Vincent Lehmuller, « La stratégie immunitaire » [archive], sur Le Grand Continent, 26 février 2020 (consulté le 27 février 2020).
- Coronavirus du syndrome respiratoire du Moyen-Orient (MERS-CoV pour Middle East respiratory syndrome coronavirus, anciennement NCoV)
- Virologie
- Coronavirus félin
- Péritonite infectieuse féline
- Syndrome respiratoire aigu sévère lié au coronavirus
- Pneumonie aiguë
- Urgence de santé publique de portée internationale (USPPI)
- Sociétés biopharmaceutiques en développement sur un vaccin : Moderna Therapeutics, CureVac, etc.
- Pandémie de maladie à coronavirus de 2019-2020
- (en) CDC [archive], CDC Novel Coronavirus [archive] et CDC’s case definitions and guidance [archive].
- (en) CDC, Site internet (CDC) consacré au novel coronavirus [archive].
- (en) OMS, WHO Novel Coronavirus Infection—UpdateExternal [archive].
- (en) Health Protection Agency Novel Coronavirus 2012 [archive].
- (fr) Cartes situation générale [1] [archive].
- (en) ECDC, ECDC: Novel Coronavirus update to Rapid Risk AssessmentExternal [archive].
- (en) CDC Mise à jour : Severe Respiratory Illness Associated with a Novel Coronavirus—Worldwide [archive], 2012–2013 MMWR March 7, 2013/62 (Early Release), p. 1-2.
- (en) CDC Severe Respiratory Illness Associated with a Novel Coronavirus — Saudi Arabia and Qatar [archive], 2012 MMWR October 12, 2012/61, p. 820-820.

/https%3A%2F%2Fprofilepics.canalblog.com%2Fprofilepics%2F4%2F2%2F426588.jpg)






/image%2F0964619%2F20240518%2Fob_e065e9_festival-du-livre-1920x1080-4-24-ecran.jpg)
/image%2F0964619%2F20240506%2Fob_4f0709_image-0991366-20181104-ob-95e079-jacqu.jpg)
/https%3A%2F%2Fstorage.canalblog.com%2F75%2F17%2F505612%2F129406040.jpeg)
/https%3A%2F%2Fstorage.canalblog.com%2F09%2F46%2F497307%2F133747489_o.jpg)